



業(ye) 務谘詢
中國:
Email: marketing@boboandtiantian.com
業(ye) 務谘詢專(zhuan) 線:400-780-8018
(僅(jin) 限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(781)535-1428(U.S.)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com



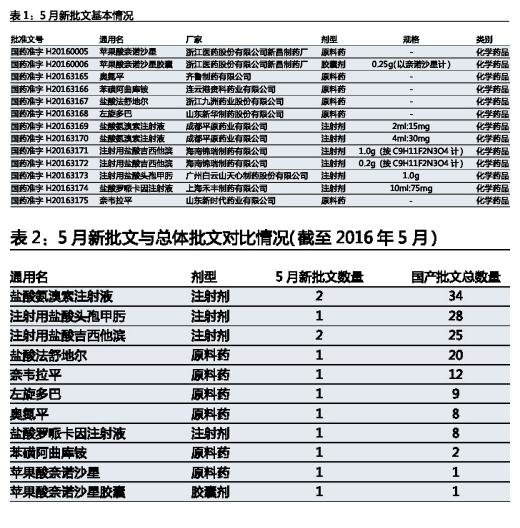
根據CFDA公布的信息,2016年5月批出13個(ge) 新國產(chan) 批文和1個(ge) 新進口批文。所有新批文全是化學藥品。按注冊(ce) 分類統計,13個(ge) 國產(chan) 批文中有2個(ge) 批文是1.1類,其它批文全部都是6類。按劑型統計分析,隻有1個(ge) 口服劑型獲批,注射劑和原料藥各有6個(ge) 批文。
1類新藥是蘋果酸奈諾沙星,膠囊劑和原料藥同時獲批,生產(chan) 廠家是浙江醫藥股份有限公司新昌製藥廠。該產(chan) 品是2016年第一個(ge) 獲批的1類新藥,用於(yu) 治療社區獲得性肺炎。浙江醫藥股份有限公司新昌製藥廠從(cong) 台灣太景公司獲得了“奈諾沙星”在中國的專(zhuan) 利權獨占許可和相關(guan) 新藥技術。據相關(guan) 資料介紹,奈諾沙星是全球首個(ge) 新型無氟喹諾酮藥物,具有極強組織穿透力,較莫西沙星更有競爭(zheng) 優(you) 勢,對多數呼吸道病原菌有很好的殺菌活性。但在“限抗”的大背景下,新品種的抗感染藥物能否突出重圍,還需看廠家的臨(lin) 床推廣力度以及藥品在臨(lin) 床上的療效反饋。如果新品種未能比老品種更有效更安全,將很難有市場生存空間。
其它獲批的新批文中,鹽酸氨溴索注射液、注射用鹽酸頭孢甲肟、注射用鹽酸吉西他濱都已有超過20個(ge) 生產(chan) 批文,所以對市場影響有限。
 相關新聞
相關新聞