



業(ye) 務谘詢
中國:
Email: marketing@boboandtiantian.com
業(ye) 務谘詢專(zhuan) 線:400-780-8018
(僅(jin) 限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(781)535-1428(U.S.)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com



必威betway网址擁有專(zhuan) 業(ye) 的製劑技術平台和具有豐(feng) 富經驗的專(zhuan) 業(ye) 團隊,竭誠為(wei) 客戶提供一站式、係統化的製劑必威客户端,滿足客戶在不同研發階段的需求,致力於(yu) 在固體(ti) 製劑、半固體(ti) 製劑、液體(ti) 製劑和滅菌製劑等提供合同必威客户端,在緩控釋製劑、微粒製劑以及蛋白質和多肽藥物製劑有豐(feng) 富的研發經驗,並有多個(ge) 成熟產(chan) 品移交給客戶,另外我們(men) 還可以同時申報FDA和CFDA以及EMEA。

抑菌效力方法開發(樣品量 20g/批,一個批次)
抑菌效力方法驗證(樣品量 80g/批,三個批次)
抑菌效力測試(3 個批次產品,樣品量 40g/批)
注:抑菌效力試驗費用需根據具體(ti) 項目和相關(guan) 人員溝通後獲得。
表 1 培養(yang) 基適用性檢查、方法適用性試驗、抑菌效力測定用的試驗菌培養(yang) 條件
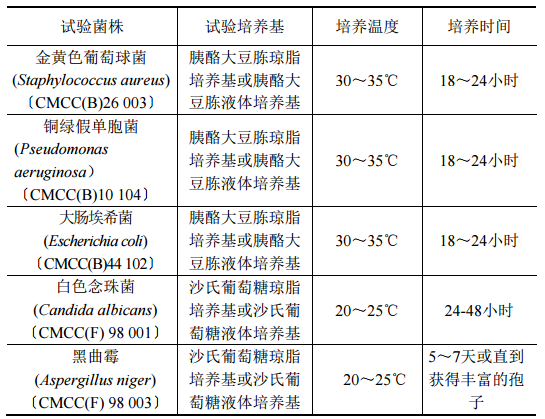
新鮮菌體(ti) 培養(yang) 見表 1,銅綠假單胞菌、金黃色葡萄球菌、大腸 埃希菌、白色念珠菌若為(wei) 瓊脂培養(yang) 物,加入適量的 0.9%無菌氯化鈉溶液將瓊脂 表麵的培養(yang) 物洗脫,並將菌懸液移至無菌試管內(nei) ,然後用0.9%無菌氯化鈉溶液 衝(chong) 洗並製成每1ml含菌數約為(wei) 108 cfu 的菌懸液;若為(wei) 液體(ti) 培養(yang) 物,離心收集菌體(ti) ,用 0.9%無菌氯化鈉溶液衝(chong) 洗並製成每1ml含菌數約為(wei) 108cfu的菌懸液。取黑曲黴的新鮮培養(yang) 物加入3~5ml 含 0.05%(ml/ml)聚山梨酯80的0.9%無菌氯 化鈉溶液,將孢子洗脫,然後,用適宜方法吸出孢子懸液至無菌試管內(nei) ,加入適量的含 0.05%(ml/ml)聚山梨酯 80 的0.9%無菌氯化鈉溶液製成每 1ml 含孢子數108cfu 的孢子懸液。測定1ml菌懸液中所含的菌數。菌液製備後若在室溫下放置,應在2小時內(nei) 使用;若保存在 2~8℃,可在24小時內(nei) 使用。黑曲黴的孢子懸液可保存在2~8℃,在 1 周內(nei) 使用。 供試品接種 抑菌效力可能受試驗用容器特征的影響,如容器的材質、形狀、體(ti) 積及封口的方式等。因此,隻要供試品每個(ge) 包裝容器的裝量足夠試驗用,同時 容器便於(yu) 按無菌操作技術接入試驗菌液、混合及取樣等,一般應將試驗菌直接接種於(yu) 供試品原包裝容器中進行貯存。若因供試品的性狀或每個(ge) 容器裝量等因素需 將供試品轉移至無菌容器時,該容器的材質不得影響供試品的特性(如吸附作用),特別應注意不得影響供試品的pH,pH 對抑菌劑的活性影響很大,同時容 器的口徑大小應便於(yu) 供試品的轉移及混勻。 取包裝完整的供試品至少5份,直接接種試驗菌,或取適量供試品分別轉移至5個(ge) 適宜的無菌容器中(若試驗菌株數超過 5 株,應增加相應的供試品份數),每一容器接種一種試驗菌,1g或1ml供試品中接菌量為(wei) 105~106cfu,接種菌液 的體(ti) 積不得超過供試品體(ti) 積的 1%,充分混合,使供試品中的試驗菌均勻分布,然後置 20~25℃避光貯存。
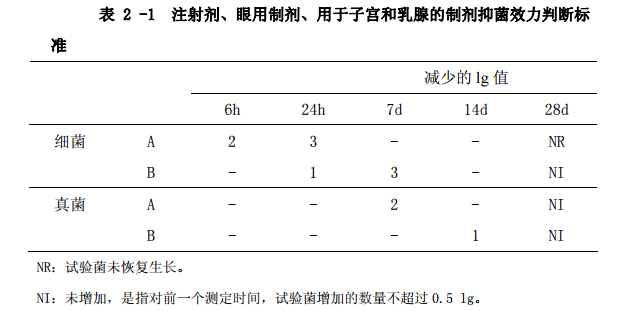
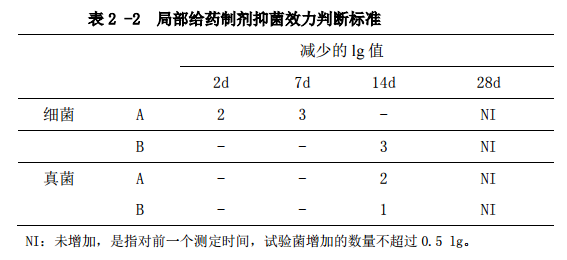
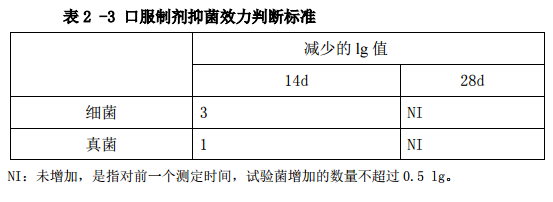
根據產(chan) 品類型,按表 2-1、表 2-2、表 2-3 規定的間隔時間, 分別從(cong) 上述每個(ge) 容器中取供試品 1ml(g),測定每份供試品中所含的菌數,測定細 菌用胰酪腖大豆瓊脂培養(yang) 基,測定真菌用沙氏葡萄糖瓊脂培養(yang) 基。存活菌數測定 方法及方法適用性試驗照微生物限度檢查法(附錄ⅩⅢ C)進行,方法適用性試驗 用菌株見表 1,菌液製備同培養(yang) 基適用性檢查,方法適用性試驗試驗菌的回收率 不得低於(yu) 70%。 根據存活菌數測定結果,計算 1ml(g)供試品各試驗菌所加的菌數及各間隔時 間的菌數,並換算成 lg 值,試驗結果按有效數字的修約規則進舍,保留小數點 後 1 位有效數字。 結果判斷 供試品抑菌效力評價(jia) 標準見表 2-1、表 2-2、表 2-3,表中的“減 少的 lg 值”是指各間隔時間測定的菌數lg值與(yu) 1ml(g)供試品中接種的菌數lg值 的相差值。表中”A”是指應達到的抑菌效力標準,特殊情況下,如抑菌劑可能增 加不良反應的風險,那至少應達到“B”的抑菌效力標準。
以上是關(guan) 於(yu) 抑菌效力試驗,抑菌效力檢查的相關(guan) 內(nei) 容,內(nei) 容來源於(yu) 必威betway网址官網。
郵箱:marketing@boboandtiantian.com
電話:02158591500
 相關新聞
相關新聞